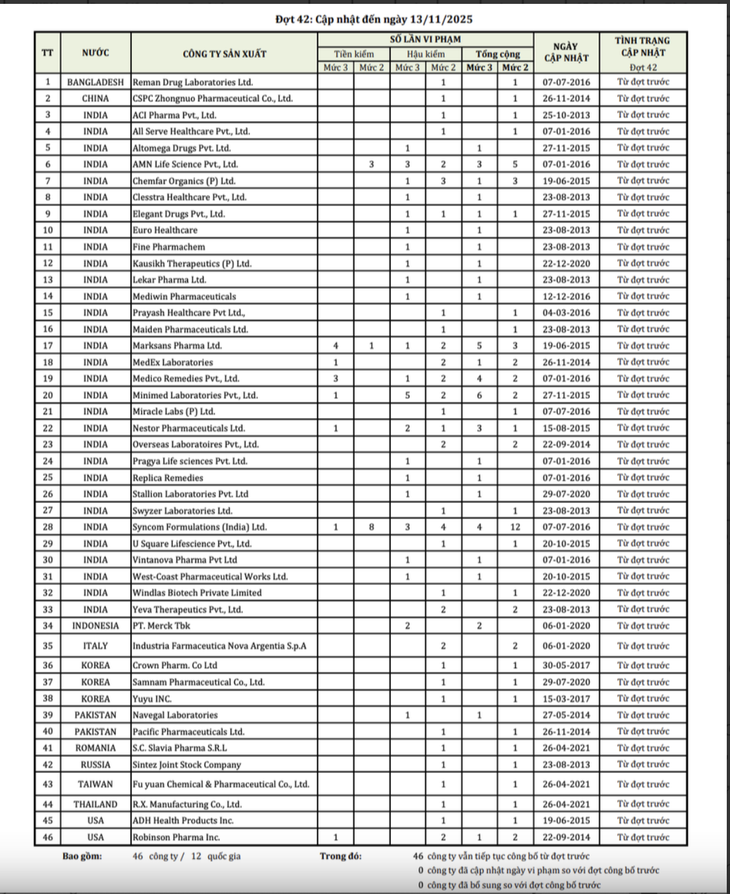
Liste de 46 sociétés pharmaceutiques étrangères dont les médicaments ne respectent pas les normes de qualité, mise à jour au 13 novembre 2025 - Photo : Département de l'administration des médicaments.
Les 46 entreprises, réparties dans 12 pays, présentaient toutes des cas de récurrences multiples, le nombre le plus élevé d'entreprises ayant connu jusqu'à 12 récurrences.
L'Administration vietnamienne des médicaments vient d'envoyer un document aux services de santé des provinces et des villes ainsi qu'aux sociétés importatrices de médicaments afin de mettre en œuvre la réglementation du ministère de la Santé concernant la publication, la mise à jour et la radiation des noms de la liste des établissements de fabrication de médicaments non conformes aux normes de qualité.
En conséquence, sur la base des résultats du contrôle de la qualité des médicaments en circulation, de l'examen des installations détenant des médicaments non conformes et des installations de fabrication de médicaments étrangères susceptibles d'être retirées de la liste de celles tenues de prélever des échantillons pour des tests de qualité sur 100 % des lots de médicaments importés, le Département de l'administration des médicaments annonce la liste des entreprises étrangères détenant des médicaments non conformes.
Par conséquent, dans cette liste, les entreprises indiennes demeurent celles du pays comptant le plus grand nombre d'entreprises en infraction. Plusieurs sociétés apparues entre 2013 et 2015 figurent toujours sur la liste de pré-inspection.
Outre le groupe important venu d'Inde, de nombreuses entreprises du Bangladesh, de Chine, d'Indonésie, de Corée du Sud, du Pakistan, des États-Unis, d'Italie et de Roumanie continuent également de faire l'objet d'une surveillance spéciale.
Les laboratoires pharmaceutiques Reman du Bangladesh, CSPC Zhongnuo de Chine, PT. Merck Tbk d'Indonésie et Crown Pharm et Yuyu Inc. de Corée du Sud ont tous été reconnus coupables lors de précédentes inspections, mais n'ont pas encore satisfait aux exigences pour que la pré-inspection soit levée.
Cette liste comprend deux entreprises américaines, ADH Health Products et Robinson Pharma, qui présentent des infractions aux normes de qualité, tant avant qu'après inspection.
Les entreprises figurant sur cette liste doivent effectuer des tests de qualité par échantillonnage sur 100 % des lots de médicaments importés (pré-inspection).
Outre la liste des infractions, l'Agence nationale de sécurité du médicament a également indiqué que 98 entreprises de 16 pays avaient été retirées de la liste de surveillance après avoir achevé la période de pré-inspection et qu'aucune nouvelle infraction n'avait été constatée.
L'Administration des médicaments du Vietnam demande aux départements de la santé des provinces, des villes et des secteurs de la santé de donner instruction aux unités de gestion, d'inspection et de contrôle des médicaments relevant de leur compétence de procéder à des inspections et de superviser le respect des réglementations relatives au contrôle de la qualité des médicaments importés en circulation dans leur zone de gestion, et de prendre des mesures à l'encontre des organisations ou des individus qui enfreignent la réglementation en vigueur.
Source : https://tuoitre.vn/danh-sach-46-cong-ty-duoc-nuoc-ngoai-co-thuoc-vi-pham-chat-luong-20251203160328166.htm


































![[Photo] Défilé pour célébrer le 50e anniversaire de la fête nationale du Laos](/_next/image?url=https%3A%2F%2Fvphoto.vietnam.vn%2Fthumb%2F1200x675%2Fvietnam%2Fresource%2FIMAGE%2F2025%2F12%2F02%2F1764691918289_ndo_br_0-jpg.webp&w=3840&q=75)











































































Comment (0)