Αυτό πιστεύεται ότι είναι η αιτία που η μεγαλύτερη κόρη του ζευγαριού, που είναι τώρα 5 ετών, πάσχει από συγγενή υπερπλασία των επινεφριδίων.
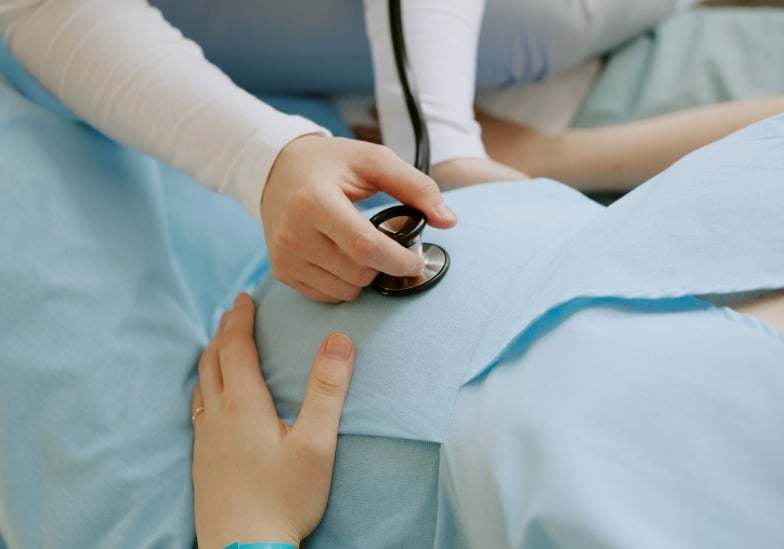
Σύμφωνα με τον Δρ. Nguyen Phuong Thao, MD, MSc, από το Κέντρο Εμβρυϊκής Ιατρικής του Γενικού Νοσοκομείου Tam Anh στην πόλη Χο Τσι Μινχ, το κοριτσάκι γεννήθηκε με ανώμαλα εξωτερικά γεννητικά όργανα που μοιάζουν με αυτά ενός άνδρα.
Τα αποτελέσματα των εξετάσεων αίματος έδειξαν ότι το επίπεδο της 17-υδροξυπρογεστερόνης, μιας στεροειδούς ορμόνης που παράγεται από τα επινεφρίδια, ήταν περισσότερο από τρεις φορές υψηλότερο από το φυσιολογικό, γεγονός που υποδηλώνει ότι το παιδί είχε υπερπλασία των επινεφριδίων.
Ο προγεννητικός και προγεννητικός γενετικός έλεγχος διαδραματίζει κρίσιμο ρόλο στον εντοπισμό φορέων γονιδίων ασθενειών και στην πρόληψη της γέννησης παιδιών με σοβαρές γενετικές διαταραχές. |
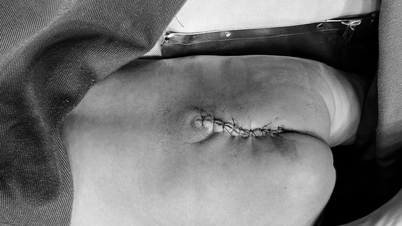
Αυτή η πάθηση εμφανίζεται λόγω διαταραχής στη σύνθεση ορμονών των επινεφριδίων, προκαλώντας οξεία επινεφριδιακή ανεπάρκεια και ανωμαλίες στα εξωτερικά γεννητικά όργανα. Παρόλο που το παιδί έχει ένα σύνολο 46 χρωμοσωμάτων XX, που σημαίνει θηλυκό, τα εξωτερικά γεννητικά όργανα είναι αρρενοποιημένα με διευρυμένη κλειτορίδα. Το παιδί έχει υποβληθεί σε επανορθωτική χειρουργική επέμβαση σε συνδυασμό με ορμονοθεραπεία για τη βελτίωση αυτής της πάθησης.
Η συγγενής υπερπλασία των επινεφριδίων είναι μια γενετική ασθένεια που κληρονομείται ως αυτοσωμικό υπολειπόμενο γονίδιο στο χρωμόσωμα 6. Η γενετική ανάλυση αποκάλυψε ότι τόσο η κα Χ. όσο και ο σύζυγός της φέρουν τη μετάλλαξη του γονιδίου CYP21A2, που σημαίνει ότι είναι φορείς της νόσου και δεν εμφανίζουν συμπτώματα. Επειδή δεν υποβλήθηκαν σε έλεγχο πριν από την εγκυμοσύνη, το γονίδιο της νόσου μεταβιβάστηκε στην κόρη τους.
Εάν εντοπιστεί νωρίς στην εγκυμοσύνη, το μωρό μπορεί να αντιμετωπιστεί ενώ βρίσκεται ακόμη στη μήτρα, βοηθώντας στην πρόληψη της αρρενοποίησης των εξωτερικών γεννητικών οργάνων. Επιπλέον, μετά τη γέννηση, μπορεί να χορηγηθεί ορμονική θεραπεία για τον περιορισμό επικίνδυνων επιπλοκών όπως η θανατηφόρα αφυδάτωση.
Γενετικά, όταν και οι δύο γονείς φέρουν το υπολειπόμενο γονίδιο που προκαλεί την ασθένεια, υπάρχει 25% πιθανότητα το δεύτερο παιδί τους να γεννηθεί υγιές, 25% πιθανότητα να έχει συγγενή υπερπλασία των επινεφριδίων ποικίλης σοβαρότητας και 50% πιθανότητα το παιδί να είναι φορέας του γονιδίου της νόσου, ενδεχομένως μεταβιβάζοντάς το στις μελλοντικές γενιές.
Αφού υποβλήθηκαν σε γενετικό έλεγχο πριν από την εγκυμοσύνη, η κα Χα και ο σύζυγός της επέλεξαν την εξωσωματική γονιμοποίηση σε συνδυασμό με τον έλεγχο εμβρύων για να διασφαλίσουν ότι θα αποκτήσουν ένα υγιές παιδί.
Ο γενετικός έλεγχος στοχεύει στον εντοπισμό υγιών φορέων του γονιδίου της νόσου, συμβάλλοντας στην πρόληψη και ελαχιστοποίηση της αρρενοποίησης των εξωτερικών γεννητικών οργάνων στα κορίτσια. Ο προγεννητικός γενετικός έλεγχος βοηθά επίσης τους γιατρούς στον έγκαιρο σχεδιασμό της θεραπείας μετά τη γέννηση, αποτρέποντας την οξεία επινεφριδιακή ανεπάρκεια.
Εάν η αρρενοποίηση στα κορίτσια αντιμετωπιστεί έγκαιρα, μπορούν να αναπτυχθούν φυσιολογικά. Αντίθετα, η καθυστερημένη διάγνωση μπορεί να οδηγήσει σε πλήρη αρρενοποίηση, προκαλώντας υπογονιμότητα και δυσκολία στη σύλληψη αργότερα στη ζωή.
Τα αγόρια με αυτή την πάθηση συχνά εμφανίζουν πρόωρη εφηβεία και καχεκτική ανάπτυξη. Οι ασθενείς χρειάζονται δια βίου θεραπεία ορμονικής υποκατάστασης και διορθωτική χειρουργική επέμβαση για δυσπλασίες των εξωτερικών γεννητικών οργάνων.
Η συγγενής υπερπλασία των επινεφριδίων έχει συχνότητα εμφάνισης περίπου 1 στις 10.000 έως 1 στις 15.000 γεννήσεις. Η νόσος μπορεί να προκαλέσει σοβαρά συμπτώματα όπως υπερκαλιαιμία, έμετο, αφυδάτωση, αργή αύξηση βάρους, υπόταση, υπογλυκαιμία, ηλεκτρολυτική ανισορροπία, κυκλοφορικό σοκ και κίνδυνο θανάτου εάν δεν αντιμετωπιστεί άμεσα.
Η νόσος οδηγεί επίσης σε ανώμαλη ανάπτυξη των γεννητικών οργάνων, όπως υπερτροφία της κλειτορίδας στα κορίτσια, διόγκωση του πέους ή μικρούς όρχεις στα αγόρια, καθώς και εφηβεία και διαταραχές της εμμήνου ρύσεως.
Οι ασθενείς διατρέχουν επίσης κίνδυνο εμφάνισης καρδιαγγειακών και μεταβολικών παθήσεων όπως υπέρταση, παχυσαρκία, δυσλιπιδαιμία, αντίσταση στην ινσουλίνη και ανισορροπία γλυκόζης. Ωστόσο, εάν εντοπιστούν και αντιμετωπιστούν επαρκώς έγκαιρα, αυτά τα παιδιά μπορούν να ζήσουν σχεδόν φυσιολογική ζωή και να έχουν τη δυνατότητα να αποκτήσουν υγιή παιδιά.
Ο προγεννητικός και προγεννητικός γενετικός έλεγχος διαδραματίζει κρίσιμο ρόλο στον εντοπισμό φορέων γονιδίων ασθενειών και στην πρόληψη της γέννησης παιδιών με σοβαρές γενετικές διαταραχές.
Με τις εξελίξεις στην εμβρυϊκή ιατρική και τη σύγχρονη γενετική τεχνολογία, πολλές επικίνδυνες ασθένειες μπορούν να ελεγχθούν αποτελεσματικά εάν εντοπιστούν έγκαιρα, παρέχοντας στα παιδιά και στις οικογένειές τους ευκαιρίες για φυσιολογική ανάπτυξη και ζωή.
Εκτός από τις προαναφερθείσες παθήσεις, η θαλασσαιμία είναι μια γενετική διαταραχή που χαρακτηρίζεται από μείωση ή ανεπάρκεια στη σύνθεση αλυσίδων σφαιρίνης στην αιμοσφαιρίνη, ένα κρίσιμο συστατικό των ερυθρών αιμοσφαιρίων. Η νόσος έχει δύο κύριες μορφές: α-θαλασσαιμία και β-θαλασσαιμία, ανάλογα με το ποια αλυσίδα σφαιρίνης επηρεάζεται.
Οι γενετικές μεταλλάξεις που προκαλούν ανεπάρκειες σφαιρίνης μπορούν να οδηγήσουν σε σοβαρές μορφές της νόσου, προκαλώντας σοβαρή αναιμία και επηρεάζοντας την υγεία και την ανάπτυξη ενός παιδιού.
Σύμφωνα με τον Δρ. Luyen Thi Thanh Nga από το Κέντρο Γενετικής Medlatec, το ποσοστό των ατόμων που φέρουν το γονίδιο της θαλασσαιμίας στο Βιετνάμ είναι αρκετά υψηλό, περίπου 13,8% σε όλες τις εθνοτικές ομάδες.
Συγκεκριμένα, ορισμένες εθνοτικές μειονοτικές ομάδες, όπως οι Tay, οι Thai και οι Muong, έχουν ποσοστό φορέων του γονιδίου α-θαλασσαιμίας που υπερβαίνει το 20%. Στη Medlatec, το 2025, η μετάλλαξη SEA είναι η πιο κοινή μορφή σε περιπτώσεις ανιχνευόμενης α-θαλασσαιμίας.
Η θαλασσαιμία είναι μια υπολειπόμενη γενετική ασθένεια, επομένως οι φορείς του γονιδίου συνήθως δεν εμφανίζουν κανένα εξωτερικό σύμπτωμα, γεγονός που καθιστά δύσκολη την ανίχνευσή του χωρίς εξειδικευμένες εξετάσεις. Εάν και οι δύο σύζυγοι φέρουν το γονίδιο της θαλασσαιμίας, ο κίνδυνος να αποκτήσουν παιδί με σοβαρή μορφή της νόσου μπορεί να φτάσει έως και το 25%.
Συνεπώς, ο προγεννητικός ή προγαμιαίος γενετικός έλεγχος είναι απαραίτητος για την παροχή συμβουλών και την πρόληψη. Στην περίπτωση της κας Κ. και του συζύγου της, ο γιατρός παρείχε συγκεκριμένες συμβουλές σχετικά με τον κίνδυνο γέννησης παιδιού με σοβαρή θαλασσαιμία και πραγματοποίησε αμνιοπαρακέντηση για προγεννητική διάγνωση. Τα αποτελέσματα έδειξαν ότι το έμβρυο είχε φυσιολογικό γονότυπο, καθησυχάζοντας την οικογένεια ότι μπορούσε να συνεχίσει την εγκυμοσύνη.
Ο γιατρός συνέστησε επίσης ότι σε επόμενες εγκυμοσύνες, το ζευγάρι θα μπορούσε να επιλέξει τη φυσική σύλληψη σε συνδυασμό με αμνιοπαρακέντηση για προγεννητική διάγνωση ή την εξωσωματική γονιμοποίηση σε συνδυασμό με εμβρυϊκό έλεγχο για την ελαχιστοποίηση των κινδύνων.
Η σοβαρή θαλασσαιμία προκαλεί χρόνια αναιμία, που απαιτεί μεταγγίσεις αίματος εφ' όρου ζωής, οδηγώντας εύκολα σε οστικές παραμορφώσεις, διόγκωση του ήπατος και του σπλήνα, καρδιακή ανεπάρκεια και ενδεχομένως πρόωρο θάνατο εάν δεν αντιμετωπιστεί έγκαιρα. Η ασθένεια επιβαρύνει επίσης σημαντικά την ψυχική και οικονομική κατάσταση των οικογενειών και της κοινωνίας.
Επομένως, ο έλεγχος του γονιδίου της θαλασσαιμίας όχι μόνο βοηθά στην έγκαιρη ανίχνευση ατόμων που φέρουν το γονίδιο της νόσου, αλλά βοηθά επίσης τα ζευγάρια να σχεδιάσουν έναν ασφαλή τοκετό, ελαχιστοποιώντας τον κίνδυνο της νόσου για τις μελλοντικές γενιές. Πρόκειται για ένα αποτελεσματικό προληπτικό μέτρο και θα πρέπει να διαδοθεί ευρέως στην κοινότητα.
Πηγή: https://baodautu.vn/sang-loc-truoc-sinh-giup-ngan-ngua-hieu-qua-di-tat-cho-tre-d331979.html









































![[Βίντεο] Η τέχνη της δημιουργίας λαϊκών ζωγραφικών έργων Dong Ho έχει εγγραφεί από την UNESCO στον Κατάλογο των Τεχνών που Χρειάζονται Επείγουσα Προστασία.](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/12/10/1765350246533_tranh-dong-ho-734-jpg.webp)




































































Σχόλιο (0)