米国食品医薬品局(FDA)は鎌状赤血球症の治療に画期的な遺伝子編集療法を承認した。
FDAの決定は12月9日に行われた。承認された2つの治療法は、ノーベル賞を受賞したCRISPR遺伝子編集技術に基づくCasgevyと、無害なウイルスを使用して遺伝子を編集するLyfgeniaと呼ばれる。
Casgevyは、Vertex Pharmaceuticals(米国)とCRISPR Therapeutics(スイス)の2社によって製造されています。この薬剤は、鎌状赤血球症およびサラセミアを患う12歳以上の患者の幹細胞における欠陥遺伝子を修復する効果があります。
どちらの疾患もヘモグロビン遺伝子の欠陥によって引き起こされます。遺伝子治療は通常数百万ドルの費用がかかり、多くの患者には手が届きません。製造元のVertex Pharmaceuticals社は、価格を可能な限り低く抑えるよう取り組んでいます。
FDAによる今回の承認は、英国の医薬品・医療製品規制庁(MHRA)が11月にこの治療法を承認したことを受けて行われた。
一方、Lyfgeniaは遺伝子導入を用いて遺伝子を編集する。患者の血液幹細胞を改変し、遺伝子由来のヘモグロビンを生成する。FDAによると、このヘモグロビンを赤血球に加えることで、鎌状赤血球症のリスクを低減する。
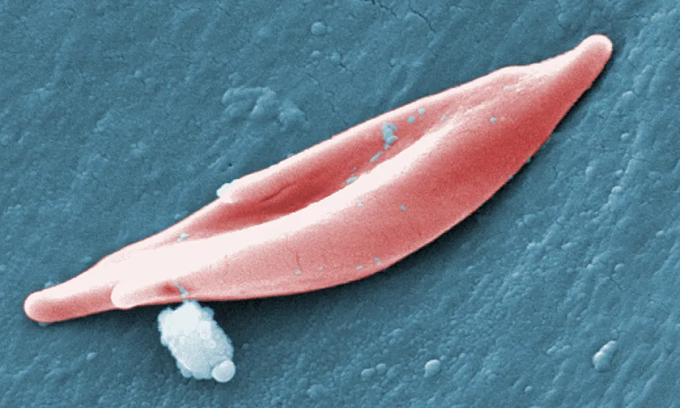
鎌状の赤血球。写真: CDC
「これらは、鎌状赤血球症患者の遺伝子治療分野における大きな進歩です。人生を変える可能性は非常に大きいです」と、FDA生物製剤評価研究センター所長のピーター・マークス氏は述べた。
FDAのニコル・ベルダン博士によると、遺伝子治療は、特に治療の選択肢が限られている希少疾患の患者にとって、治療をより的確かつ効果的にすることができるという。
FDAは「この分野を前進させることに非常に興奮している」と彼女は付け加えた。なぜならFDAは、この病気によって生活がひどく乱された人々を助けるからだ。
この承認により、鎌状赤血球症の患者約1万6000人が治療の選択肢を得ることになります。この疾患は、アメリカで約10万人、世界で770万人以上が罹患しており、そのほとんどがアフリカ系およびカリブ海諸国出身者です。鎌状赤血球症は希少かつ衰弱性で生命を脅かす血液疾患であり、多くの患者が未だ治療ニーズを満たせていません。
鎌状赤血球症の患者は、典型的な凹型の丸い血球ではなく、細長い鎌状の血球を呈します。この奇形は血管に詰まり、酸素供給を阻害し、激しい痛み、脳卒中、臓器障害を引き起こします。
トゥク・リン氏( AFP、AP通信による)
[広告2]
ソースリンク



















![[インフォグラフィック] 大気汚染と保健省からの勧告](https://vphoto.vietnam.vn/thumb/402x226/vietnam/resource/IMAGE/2025/12/05/1764950568593_screen-shot-2025-12-05-at-222015-png.webp)
























































































コメント (0)